Kỹ thuật tạo hình tham số trong thời gian thực của siêu âm tương phản chẩn đoán tổn thương gan ác tính
BS NGUYỄN THIỆN HÙNG dịch
TRUNG TÂM Y KHOA MEDIC HÒA HẢO
Thành phố Hồ Chí Minh
(từ Eric Barnes: Contrast US Processing Tools Shows Malignant Liver Lesions, AuntMinnie.com, 30 tháng 7 năm 2010).
Các nhà nghiên cứu Thụy Sĩ đã phát triển một kỹ thuật hình ảnh tham số trong thời gian thực (real-time parametric imaging technique) bằng siêu âm tăng cường tương phản (contrast-enhanced ultrasound) để phân biệt không xâm lấn tổn thương gan lành tính và ác tính dễ sử dụng. Trong lần áp dụng lâm sàng đầu tiên, phương thức này có độ đặc hiệu và độ nhạy cao trong một nghiên cứu đoàn hệ.
Phân biệt không xâm lấn tổn thương gan lành tính và ác tính bằng siêu âm là mục tiêu nghiên cứu trọng điểm, và được xem là tiềm năng hứa hẹn nhất của siêu âm tăng cường tương phản.
"Có thể phân biệt tổn thương bằng cách xem sự hấp thụ chất tương phản của nó so với nhu mô bình thường xung quanh", ông Nicolas Rognin, PhD, từ Research Bracco tại Geneva, đã trình bày như trên tại cuộc họp Computer hỗ trợ Radiology và Phẫu thuật (CARS), 2010 tháng Sáu cũng tại Geneva.
Sau khi tiêm 1 bolus chất tương phản, đặc điểm của tổn thương gan có kiểu động học mạch máu (DVP, dynamic vascular patterns) khi so sánh với nhu mô lành xung quanh. Theo các tín hiệu video hấp thu độ tương phản trong gan ghi lại được tuyến tính hoá, động học hấp thu chất tương phản được thể hiện bằng đơn vị echo-cường độ (echo-power units) như là một hàm của thời gian.
Có hai loại tổn thương, lành tính hoặc ác tính, mỗi loại tách thành hai lớp. Trong ung thư tế bào gan nguyên phát, DVP của nó cho thấy tăng cường mạnh trong giai đoạn động mạch so với nhu mô lành xung quanh, tiếp theo là thì thải thuốc trong giai đoạn tĩnh mạch cửa, và trở nên kém tăng cường (hypoenhanced) rõ trong giai đoạn trễ.
Để làm cho những khác biệt thang xám này dễ thấy hơn, các nghiên cứu trước đó đã phát triển kỹ thuật xử lý ảnh để tăng cường những trình tự DVP này trong hình ảnh tái tạo. Phương pháp này giúp chẩn đoán tổn thương, nhưng chẩn đoán hạn chế chỉ với một hình tại một thời điểm.
Trên, phân tích DVP trong siêu âm dùng để phân biệt lành tính và ác tính từ kiểu dòng chảy trong tổn thương gan khu trú.
(FNH= focal hyperplasia, nốt tái tạo)
HCC= ung thư tế bào gan nguyên phát).
Dưới, một hình của phương pháp postprocessing chẩn đoán kiểu dòng chảy bằng màu từ một nghiên cứu trước đó của nhóm rendered DVP khác biệt dễ thấy hơn. Tuy nhiên, phương pháp này bị hạn chế trong việc mô tả một hình duy nhất ở một thời điểm. © Bracco Switzerland 2010.
Trong nghiên cứu này, "mục tiêu là để cung cấp tất cả các thông tin lâm sàng có liên quan ở một hình ảnh duy nhất," một kỳ công thực hiện bằng cách " áp dụng phân loại pixel để vẽ bản đồ chữ ký mạch máu vào một hình ảnh tham số," Rognin nói.
Kỹ thuật vẽ bản đồ tham số động học (parametric dynamic mapping) bao gồm bốn bước chính:
1.Tiền xử lý (Preprocessing): Dữ liệu video chuyển đổi không gian để bù cho bất kỳ chuyển động nào trong mặt phẳng (in-plane motion), và sau đó tuyến tính hóa (linearized) để lấy được tín hiệu echo-cường độ ở cấp độ pixel.
2.Làm mịn tín hiệu (Signal smoothing): Tín hiệu echo-cường độ này sau đó được làm nhẵn bằng cách sử dụng một kỹ thuật vẽ đường cong khớp với các điểm đã cho (curve fitting) với một mô hình chức năng bolus tưới máu.
3.Trừ tín hiệu (Signal subtraction): Các tín hiệu " khác biệt " được tính bằng cách trừ đi các tín hiệu tham khảo từ các tín hiệu echo-cường độ được mềm hoá (smoothed).
4.Phân loại pixel (Pixel classification): Điểm ảnh được phân thành bốn lớp theo cực của tín hiệu khác biệt theo thời gian.
Sử dụng siêu âm tăng cường tương phản, hemangiomas lành tính thường hyperenhanced vào mọi lúc, trong khi di căn ác tính thường hypervascular biểu hiện hyperenhancement trong giai đoạn động mạch và theo sau là hypoenhancement trong giai đoạn tĩnh mạch cửa. Các tín hiệu khác biệt trong hemangioma trình bày một chữ ký mạch máu đơn cực, trong khi tín hiệu khác biệt của di căn hypervascular có chữ ký mạch máu lưỡng cực.
Biểu đồ phân loại pixel sử dụng màu xanh lá đại diện cho đơn cực dương (chữ ký hyperenhanced thường trực). Màu xanh dương miêu tả đơn cực âm (chữ ký hypoenhanced thường trực), trong khi màu đỏ đại diện cho kết quả dương lưỡng cực (hyperenhancement, theo chữ ký hypoenhancement) và màu vàng được miêu tả âm lưỡng cực (hypoenhancement, theo chữ ký hyperenhancement).
Do đó, tổn thương ác tính xuất hiện là các khu vực màu đỏ, còn tổn thương lành tính có màu xanh lá hoặc màu vàng. Khi phân tích, trình tự phân tích tương phản sau đó được tổng hợp như bản đồ không gian của chữ ký mạch máu dùng để chẩn đoán loại tổn thương.
Các nhà nghiên cứu dùng kỹ thuật hình ảnh tham số DVP để đánh giá 146 tổn thương gan (113 ác tính và 33 lành tính), hình ảnh hoá với chỉ số cơ học thấp (MI, mechanical index) trong thời gian thực bằng siêu âm tương phản chuyên biệt sau khi tiêm bolus 2,4 mL một chất tương phản microbubble (SonoVue, Bracco, Milan).
Hemangiomas (lành tính) thường hyperenhanced vào mọi lúc, trong khi di căn hypervascular (ác tính) thường trình bày một hyperenhancement trong giai đoạn động mạch, theo sau là một hypoenhancement trong giai đoạn tĩnh mạch cửa. Mã màu của các loại tổn thương ác tính hoặc lành tính được thực hiện bằng cách phân tích sự khác biệt tín hiệu, được xác định bằng cách trừ đi các tín hiệu tham khảo từ các tín hiệu echo-cường độ mềm hoá (smoothed) trong hình ảnh siêu âm. Các tín hiệu khác biệt trong hemangioma trình bày một chữ ký mạch máu đơn cực, trong khi các tín hiệu khác biệt di căn hypervascular có một chữ ký mạch máu lưỡng cực.
Trong bảng dưới đây, chữ ký mạch máu được phân loại thành bốn lớp theo tín hiệu khác biệt phân cực tương ứng theo thời gian. Màu khác nhau được sử dụng để hiển thị các điểm ảnh trong các lớp khác nhau.
Để kiểm định những phát hiện từng trường hợp được đối chiếu với CT, MRI, hoặc sinh thiết.
Các tổn thương đã được quét bằng cách sử dụng siêu âm tương phản có chỉ số cơ học MI (mechanic index) thấp trong thời gian thực trên một trong một số máy siêu âm, trong đó có HDI 5000 và iU22 (Philips Healthcare , Andover, MA), SSD-5500 (Aloka , Tokyo), hoặc Sequoia 512 (Siemens Healthcare, Erlangen, Germany).
Các hình ảnh tham số DVP đã được đọc bởi một bác sĩ lâm sàng mù với các kết quả bằng cách sử dụng màu đỏ như là một tiêu chí về bệnh ác tính. Phương pháp mang lại độ nhạy 97%, độ đặc hiệu 91% đối với bệnh ác tính.
Trong khi đó, một nghiên cứu đa trung tâm của siêu âm tăng cường tương phản mà không sử dụng phương pháp lập bản đồ có độ nhạy 91% và độ đặc hiệu 86% ( American Journal of Roentgenology, tháng 6 năm 2006, Vol. 186:6, tr. 1551-1559).
"Các điểm thu được hiệu quả cao với hình ảnh tham số DVP chứng minh tiềm năng của phương pháp này để tăng độ tin cậy trong chẩn đoán tổn thương gan khu trú," Rognin lưu ý rằng các kết quả thuận lợi so với y văn.
Ngoài việc cung cấp một phương pháp chẩn đoán đơn giản là tìm các khu vực màu đỏ như chỉ báo của bệnh ác tính, kỹ thuật này có lợi thế là ít tốn thời gian hơn so với phương pháp hiện thời là xem xét trình tự của toàn bộ các hình ảnh tương phản. Chỉ thực hiện mất khoảng hai phút cho mỗi trường hợp.
Các nhà nghiên cứu dự định nghiên cứu phân đoạn tự động nhu mô bình thường để giảm thiểu phụ thuộc vào người đọc kết quả các bản đồ tham số, do đó tiếp cận chẩn đoán siêu âm tương phản tổn thương gan có máy tính hỗ trợ.
"Trong tương lai, hình ảnh học tương phản 4D có khả năng trở nên phổ biến," Rognin nói. "Việc xem xét lại trình tự như thế có thể trở nên khá tẻ nhạt, do đó, phần mở rộng dữ liệu thể tích của hình ảnh tham số DVP có thể trở thành một công cụ rất có giá trị cho bác sĩ."
Bốn trường hợp lâm sàng cho thấy làm thế nào hình ảnh tham số DVP cho phép tạo điều kiện đặc điểm tổn thương như là lành hay ác tính trong bốn ví dụ lâm sàng điển hình, với tổn thương ác tính xuất hiện với màu đỏ, không giống như các tổn thương lành tính xuất hiện với màu xanh lá hoặc màu xanh lá - màu vàng.
Các nhà nghiên cứu cũng có kế hoạch đánh giá kỹ thuật của họ rộng rãi hơn trong một nhóm bệnh nhân lớn hơn.
Tổng số lượt xem trang
Thứ Sáu, 6 tháng 8, 2010
Thứ Năm, 5 tháng 8, 2010
SIÊU ÂM ĐO BỀ DÀY VỎ THẬN / Renal Cortical Thickness Measured at Ultrasound
AJR 2010; 195:W146-W149
© American Roentgen Ray Society
SIÊU ÂM ĐO BỀ DÀY VỎ THẬN TRONG ĐÁNH GIÁ CHỨC NĂNG THẬN MẠN TÍNH
Renal Cortical Thickness Measured at Ultrasound: Is It Better Than Renal Length as an Indicator of Renal Function in Chronic Kidney Disease?, Michael D. Beland, Nicholas L. Walle, Jason T. Machan and John J. Cronan
1 Department of Diagnostic Imaging, Rhode Island Hospital, Warren Alpert Medical School of Brown University, 593 Eddy St., Providence, RI 02903.
2 Departments of Biostatistics and Research, Orthopaedics, and Surgery, Rhode Island Hospital, Warren Alpert Medical School of Brown University, Providence, RI.
OBJECTIVE. Mục tiêu nghiên cứu là xác định tương quan giữa bề dày vỏ thận hay chiều dài thận đo bằng siêu âm với mức độ tổn thương thận mạn tính.
MATERIALS and METHODS. Từ 10-12/2007, có 25 bệnh nhân (12 nam và 12 nữ, tuổi trung bình là 73) được xác định là bệnh thận mạn tính nhưng chưa thẩm tách thận (dialysis, chạy thận nhân tạo). Các bệnh nhân này ở cùng bệnh viện và được siêu âm thận và định lượng creatinines 3 lần trong 90 ngày. Lượng creatinines thấp nhất được dùng để đánh giá tốc độ lọc cầu thận (estimated glomerular filtration rate, eGFR) dùng cả công thức Cockcroft-Gault (CG) và Modification of Diet in Renal Disease Study (MDRD). 3 người làm siêu âm đều mù với kết quả chức năng thận. Bề dày vỏ thận được đo qua mặt cắt sagittale qua tháp thận thẳng góc với vỏ thận. Chiều dài thận đo từ cực này đến cực kia.Tương quan tuyến tính được dùng để phân tích thống kê.
RESULTS. Bề dày vỏ thận trung bình là 5,9mm (3,2-11mm), Chiều dài thận trung bình là 10cm (7,2-12,4mm). Creatinine tối thiểu trung bình là 2,1mg/dL. Tốc độ lọc cầu thận là 34,8mL/min (10,6-99,4mL/min). Có tương quan có ý nghĩa thống kê giữa eGFR và bề dày vỏ thận cả ở CG (p = 0.0001) và MDRD (p = 0,005). Có tương quan có ý nghĩa thống kê giữa CG và chiều dài thận (p = 0,003), nhưng không có tương quan giữa MDRD và chiều dài thận (p = 0,08).
CONCLUSION. Bề dày vỏ thận đo bằng siêu âm tương quan chặt với eGFR hơn với chiều dài thận. Báo cáo bề dày vỏ thận ở bệnh nhân thận mạn tính chưa thẩm tách thận nên được chấp nhận.
Keywords: chronic kidney disease • estimated glomerular filtration rate • renal cortex • renal failure • ultrasound
© American Roentgen Ray Society
SIÊU ÂM ĐO BỀ DÀY VỎ THẬN TRONG ĐÁNH GIÁ CHỨC NĂNG THẬN MẠN TÍNH
Renal Cortical Thickness Measured at Ultrasound: Is It Better Than Renal Length as an Indicator of Renal Function in Chronic Kidney Disease?, Michael D. Beland, Nicholas L. Walle, Jason T. Machan and John J. Cronan
1 Department of Diagnostic Imaging, Rhode Island Hospital, Warren Alpert Medical School of Brown University, 593 Eddy St., Providence, RI 02903.
2 Departments of Biostatistics and Research, Orthopaedics, and Surgery, Rhode Island Hospital, Warren Alpert Medical School of Brown University, Providence, RI.
OBJECTIVE. Mục tiêu nghiên cứu là xác định tương quan giữa bề dày vỏ thận hay chiều dài thận đo bằng siêu âm với mức độ tổn thương thận mạn tính.
MATERIALS and METHODS. Từ 10-12/2007, có 25 bệnh nhân (12 nam và 12 nữ, tuổi trung bình là 73) được xác định là bệnh thận mạn tính nhưng chưa thẩm tách thận (dialysis, chạy thận nhân tạo). Các bệnh nhân này ở cùng bệnh viện và được siêu âm thận và định lượng creatinines 3 lần trong 90 ngày. Lượng creatinines thấp nhất được dùng để đánh giá tốc độ lọc cầu thận (estimated glomerular filtration rate, eGFR) dùng cả công thức Cockcroft-Gault (CG) và Modification of Diet in Renal Disease Study (MDRD). 3 người làm siêu âm đều mù với kết quả chức năng thận. Bề dày vỏ thận được đo qua mặt cắt sagittale qua tháp thận thẳng góc với vỏ thận. Chiều dài thận đo từ cực này đến cực kia.Tương quan tuyến tính được dùng để phân tích thống kê.
Bề dày vỏ thận (cortical thickness) là khoảng cách giữa bao thận và bờ viền ngoài của tháp thận.
Bề dày chủ mô thận (parenchymal thickness) là khoảng cách giữa bao thận và đường viền của xoang thận.
CONCLUSION. Bề dày vỏ thận đo bằng siêu âm tương quan chặt với eGFR hơn với chiều dài thận. Báo cáo bề dày vỏ thận ở bệnh nhân thận mạn tính chưa thẩm tách thận nên được chấp nhận.
Keywords: chronic kidney disease • estimated glomerular filtration rate • renal cortex • renal failure • ultrasound
Thứ Ba, 3 tháng 8, 2010
GEL SIÊU ÂM và BỆNH LÝ NỘI MẠC TỬ CUNG/Gel instillation sonography advantageous in endometrial evaluation
TRUYỀN NHỎ GIỌT GEL ĐÁNH GIÁ BỆNH LÝ NỘI MẠC TỬ CUNG
Gel instillation sonography advantageous in endometrial evaluation
Reuters Health • The Doctor's Channel Daily Newscast
Gel instillation sonography advantageous in endometrial evaluation
Reuters Health • The Doctor's Channel Daily Newscast
Khảo sát siêu âm bệnh lý nội mạc tử cung với truyền nhỏ giọt gel để làm căng đầy buồng tử cung dễ thực hiện hơn truyền saline là một báo cáo của nhóm tác giả Bỉ. Dr. Thierry Van den Bosch và cộng sự, University Hospitals Leuven, cho biết khó mà giữ cho căng tốt buồng tử cung với saline và có thể gieo mầm tế bào ác tính vào ổ bụng qua vòi trứng, trong khi truyền gel có thể vượt qua các vấn đề này.
Nhóm nghiên cứu đã truyền nhỏ giọt saline cho 402 phụ nữ bị chảy máu bất thường và truyền nhỏ giọt gel cho 402 người khác. Truyền gel thành công hơn: tỉ lệ thất bại của truyền saline là 5,0% so với truyền gel là 1,8% và tỷ lệ thất bại tương ứng do làm căng không đầy đủ buồng tử cung là 1,5% (saline) so với 0,3% (gel).
Về bệnh học, kết quả tăng sản nội mạc, pôlyp, ung thư hay nhân xơ lòng tử cung là 49% của truyền saline so với truyền gel là 40,2%, khác biệt không có ý nghĩa thống kê. Độ nhạy lần lượt là 77,8% và 85%. Giá trị tiên đoán âm tính là 79,1% của truyền nhỏ giọt saline và 88,6% của truyền nhỏ giọt gel. Bất lợi (drawback) của truyền gel là khả năng chẩn đoán lầm máu cục là polyp vì saline vốn được dùng làm sạch cục máu đông.
Nhìn chung, cả hai kỹ thuật đều khả thi và chính xác. Tuy nhiên, "Gel có một số lợi thế hơn saline: làm đầy ổn định buồng tử cung, không cần thông bóng (balloon catheters), tiện nghi bệnh nhân được cải thiện, và, về lý thuyết, nguy cơ thấp hơn lan truyền trong phúc mạc tế bào ác tính. Vì vậy, nên sử dụng truyền nhỏ giọt gel thay vì truyền nhỏ giọt saline. "
Reference:
Detection of endometrial pathology using saline infusion sonography versus gel instillation sonography: a prospective cohort study, Fertil Steril 2010.
Thứ Bảy, 3 tháng 7, 2010
HÌNH ẢNH SIÊU ÂM của GOUT/ULTRASOUND FINDINGS in GOUT: DOUBLE CONTOUR SIGN, TOPHACEOUS MATERIALS and OTHER
Các dấu hiệu siêu âm trong gout gồm:
- Dấu viền đôi (double contour sign) là 2 đường: một là dải echo dày có bề mặt không đều do tinh thể urat (monosodium urate, MSU) lắng đọng trên bề mặt sụn khớp, và đường thứ hai là đường viền vỏ xương có echo dày.
- Vùng mờ echo dày (hyperechoic cloudy area) do tinh thể urat lắng đọng trong màng hoạt dịch viêm dày. Cục tophus thường có dạng ovale như nhúm đường ướt (wet sugar clumps) ở cạnh xương và khoảng khớp, có echo kém hay echo dày, không đồng dạng, và có viền không có echo xung quanh (hay đường nối, anechoic seam).
Vùng mờ echo dày và cục tophus là 2 dạng lắng đọng tinh thể urat (tophaceous material) thường thấy ở khớp bàn đốt ngón chân (metatarsophalangeal, MTP) và khớp bàn đốt ngón tay (metacarpophalangeal, MCP).
- Khuyết xương (erosion) ở cạnh nơi lắng đọng tinh thể urat, là các chỗ vỡ của đường viền echo dày của vỏ xương.
- Phì đại màng hoạt dịch là nơi dày đồng tâm của màng hoạt dịch. Có tăng tưới máu mô màng hoạt dịch trên power Doppler ở các trường hợp không có triệu chứng lâm sàng gout cấp.

- Tụ dịch khớp có trong gout cấp tính, gout mạn tính và đợt cấp gout mạn tính.
Siêu âm có khả năng chẩn đoán gout không xâm lấn nhờ phát hiện tinh thể urat lắng đọng trên bề mặt sụn khớp (double contour sign, dấu viền đôi), các dạng lắng đọng tinh thể urat (tophaceous materials) và khuyết xương điển hình (typical erosion).
____________________________________________
Ghi chú:
1. Phương pháp chẩn đoán gout đáng tin cậy nhất là chọc hút dịch khớp và soi kính hiển vi phân cực (polarizing microscopy) để định danh tinh thể.
(Hình từ Wikipedia)
2. Giả gout (pseudogout) là thể chính của bệnh lý lắng đọng calcium pyrophosphate dihydrate (CPPD) và viêm khớp mạn. Khác với gout, CPPD lắng đọng trong trung tâm của sụn hyaline và fibrous, tạo nên một lớp trong sụn hyaline song song với vỏ xương: sụn nhiễm vôi (chondrocalcinosis). Hình ảnh siêu âm sụn nhiễm vôi là một đường echo dày không đều trong sụn hyaline.
KÍNH HIỂN VI PHÂN CỰC: Kính hiển vi quang học có hai nicon phân cực ánh sáng, đặt thẳng góc nhau: nicon phân cực đặt dưới mâm kính, nicon phân tích đặt giữa vật kính và thị kính. Mẫu đá hoặc khoáng vật mài mỏng tới bề dày 0,03 mm, được gắn bằng nhựa Canađa vào tấm thuỷ tinh và đặt trên mâm kính.
KHVPC cho phép xác định các hằng số quang học của khoáng vật (chiết suất, lưỡng chiết suất, góc quang học, màu tự nhiên, màu đa sắc của khoáng vật kim loại) và nhờ đó có thể xác định chính xác tên khoáng vật.
Tài liệu tham khảo chính:
1.R.G. Thiele and N.Schlesinger: Diagnosis of Gout by Ultrasound, Rheumatology 2007;46:1116-21.
2.Naomi Schlesinger: Diagosis of Gout: Clinical, Laboratory and Radiologic Findings, The American Journal of Managed Care, Vol 11 No sup S443-450, November 2005.
3. Stephen A Wright, Emilio Filippucci, Claire McVeigh, et al: High-Resolution Ultrasonography of the First Metatarsal Phalangeal Joint in Gout: a Controlled Study, Ann Eheum Dis 2007;66:859-864.
Chủ Nhật, 13 tháng 6, 2010
Appendiceal Mucocele : Ultrasound Findings
SIÊU ÂM U NHÀY RUỘT THỪA
U nhày ruột thừa được định nghĩa như là giãn lòng ruột thừa thành nang do tích tụ chất nhày (mucin). Là bệnh hiếm gặp, chiếm 0,2-0,3% các trường hợp cắt ruột thừa. Do sỏi phân, do carcinoid ... và quan trọng hơn do mucinous cystadenoma hoặc cystadenocarcinoma. Nếu u nhày vỡ sẽ gây ra tình trạng giả u nhày phúc mạc (pseudomyxoma peritonei). Nên cần chẩn đoán chính xác trước mổ để tiến hành phẫu thuật cẩn thận. U nhày ruột thừa được xem là một chẩn đoán phân biệt cho các trường hợp u vùng hố chậu P với ruột thừa chưa cắt bỏ. Tốt nhất là nên có chỉ định phối hợp với CT để có chẩn đoán chính xác trước mổ.
Về bệnh học u nhày ruột thừa có 4 loại. Loại thứ phát, hiếm gặp nhất, do tắc nghẽn bởi sẹo sau viêm, teo do tuổi tác, tắc bẩm sinh van Gerlach hoặc do chèn ép từ ngoài vách. Còn lại là do tăng sinh niêm mạc, hay mucinous cystadenoma hoặc mucinous cystadenocarcinoma tùy thuộc vào bệnh lý niêm mạc. Có 25% là do mucosal hyperplasia, thường giãn ít. Giãn nhiều hơn (trung bình = 40x24x20cm) là mucinous cystadenoma chiếm 60%, thường không có triệu chứng, được phát hiện tình cờ; với 20% có chất nhày ngoài ruột thừa, và nếu không có tế bào trong chất nhày tiên lượng thường tốt. Mucinous cystadenocarcinoma chiếm 10,15% được chẩn đoán bằng có tân sinh mô tuyến xâm lấn vách và có tế bào trong chất nhày phúc mạc. Loại này thường có triệu chứng. Vài tác giả cho rằng giả u nhày phúc mạc chỉ do mucinous cystadenocarcinoma. Mucinous cystadenocarcinoma cực hiếm, xuất phát từ cystadenomas, có đồng thời hoặc khác thời (metachronous) với colorectal adenoma và carcinomas. Có các báo cáo cho thấy có liên quan với các u đường tiêu hoá, u buồng trứng và u thận.
Hình ảnh siêu âm của u nhày ruột thừa:
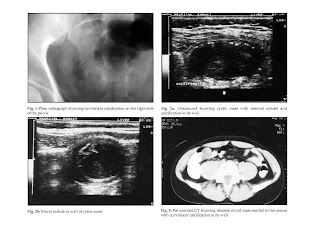
Điển hình là nang có truyền âm và tăng cường âm vách sau. Nếu nang có vôi hoá thường có bóng lưng sau nhưng ít được chú ý. Bề dày vách thay đổi, nhưng nếu vách dày hơn 6mm được xem là biến chứng của viêm ruột thừa cấp. Lòng u nhày ruột thừa không có echo (anechoic) hay có echo dày (hyperechoic) uốn sóng hay xếp từng lớp (dấu vảy hành, oignon skin sign). Lòng có vách hay có dạng polyp và đường viền không đều thường là ác tính dù dạng polyp thường có ở mucinous cystadenoma. Các chẩn đoán phân biệt của siêu âm là tụ dịch ruột non, dịch trong túi thừa đại tràng, áp xe ruột thừa hay áp xe túi thừa và nang thanh dịch mạc treo (mesenteric cyst seroma). Ở phụ nữ đang thời sinh sản chẩn đoán phân biệt còn là viêm vòi trứng hoặc thai ngoài tử cung.
Trên CT, điển hình là khối nhẳn hoặc có múi có đậm độ thấp (0-40HU). Các u nhày có dạng bất thường hay phức tạp thường là mucinous cystadenocarcinoma, với 1 nang hay nhiều nang và thành phần đặc. Có thể xâm nhiễm các cơ quan lân cận như đại tràng, bàng quang, và niệu quản. Vôi hoá dạng chấm hay đường uốn cong thường là mucinous cystadenoma, không thấy trên phim bụng không chuẩn bị. Vôi hoá không định hình thường là ác tính, do viêm mạn tính vì chất nhày kích thích. Nên tìm thêm xem có u kết hợp với u nhày ruột thừa không như u đại tràng (xuất độ 6 lần đối với colon adenocarcinoma) hay u buồng trứng tiết nhày (mucin-secreting).
U nhày ruột thừa nên được xem là chẩn đoán phân biệt cho các khối vùng hố chậu P. Để có chẩn đoán chính xác trước mổ, bắt buộc phải làm CT. Tất cả nhằm giúp phẫu thuật viên cẩn thận hơn để tránh làm vỡ u nhày ruột thừa làm rò chất nhày vào ổ bụng gây giả u nhày phúc mạc.
Xem ca 181 Vietnamese Medic Ultrasound .
Tài liệu tham khảo chính:
Aghahowa EJ, Bharati C, Al-Adwani M: Appendicular Mucocele, A Case Report, Kuwait Medical Journal, March, 2008, pp78-8
Francica G, Lapiccirella G, Giardiello C, Scarano F, Angelone C, De Marino F, Molese V: Giant Mucocele of the Appendix, J Ultrasound Med, 2006, 25:643-648.0.
U nhày ruột thừa được định nghĩa như là giãn lòng ruột thừa thành nang do tích tụ chất nhày (mucin). Là bệnh hiếm gặp, chiếm 0,2-0,3% các trường hợp cắt ruột thừa. Do sỏi phân, do carcinoid ... và quan trọng hơn do mucinous cystadenoma hoặc cystadenocarcinoma. Nếu u nhày vỡ sẽ gây ra tình trạng giả u nhày phúc mạc (pseudomyxoma peritonei). Nên cần chẩn đoán chính xác trước mổ để tiến hành phẫu thuật cẩn thận. U nhày ruột thừa được xem là một chẩn đoán phân biệt cho các trường hợp u vùng hố chậu P với ruột thừa chưa cắt bỏ. Tốt nhất là nên có chỉ định phối hợp với CT để có chẩn đoán chính xác trước mổ.
Về bệnh học u nhày ruột thừa có 4 loại. Loại thứ phát, hiếm gặp nhất, do tắc nghẽn bởi sẹo sau viêm, teo do tuổi tác, tắc bẩm sinh van Gerlach hoặc do chèn ép từ ngoài vách. Còn lại là do tăng sinh niêm mạc, hay mucinous cystadenoma hoặc mucinous cystadenocarcinoma tùy thuộc vào bệnh lý niêm mạc. Có 25% là do mucosal hyperplasia, thường giãn ít. Giãn nhiều hơn (trung bình = 40x24x20cm) là mucinous cystadenoma chiếm 60%, thường không có triệu chứng, được phát hiện tình cờ; với 20% có chất nhày ngoài ruột thừa, và nếu không có tế bào trong chất nhày tiên lượng thường tốt. Mucinous cystadenocarcinoma chiếm 10,15% được chẩn đoán bằng có tân sinh mô tuyến xâm lấn vách và có tế bào trong chất nhày phúc mạc. Loại này thường có triệu chứng. Vài tác giả cho rằng giả u nhày phúc mạc chỉ do mucinous cystadenocarcinoma. Mucinous cystadenocarcinoma cực hiếm, xuất phát từ cystadenomas, có đồng thời hoặc khác thời (metachronous) với colorectal adenoma và carcinomas. Có các báo cáo cho thấy có liên quan với các u đường tiêu hoá, u buồng trứng và u thận.
Hình ảnh siêu âm của u nhày ruột thừa:
Điển hình là nang có truyền âm và tăng cường âm vách sau. Nếu nang có vôi hoá thường có bóng lưng sau nhưng ít được chú ý. Bề dày vách thay đổi, nhưng nếu vách dày hơn 6mm được xem là biến chứng của viêm ruột thừa cấp. Lòng u nhày ruột thừa không có echo (anechoic) hay có echo dày (hyperechoic) uốn sóng hay xếp từng lớp (dấu vảy hành, oignon skin sign). Lòng có vách hay có dạng polyp và đường viền không đều thường là ác tính dù dạng polyp thường có ở mucinous cystadenoma. Các chẩn đoán phân biệt của siêu âm là tụ dịch ruột non, dịch trong túi thừa đại tràng, áp xe ruột thừa hay áp xe túi thừa và nang thanh dịch mạc treo (mesenteric cyst seroma). Ở phụ nữ đang thời sinh sản chẩn đoán phân biệt còn là viêm vòi trứng hoặc thai ngoài tử cung.
Trên CT, điển hình là khối nhẳn hoặc có múi có đậm độ thấp (0-40HU). Các u nhày có dạng bất thường hay phức tạp thường là mucinous cystadenocarcinoma, với 1 nang hay nhiều nang và thành phần đặc. Có thể xâm nhiễm các cơ quan lân cận như đại tràng, bàng quang, và niệu quản. Vôi hoá dạng chấm hay đường uốn cong thường là mucinous cystadenoma, không thấy trên phim bụng không chuẩn bị. Vôi hoá không định hình thường là ác tính, do viêm mạn tính vì chất nhày kích thích. Nên tìm thêm xem có u kết hợp với u nhày ruột thừa không như u đại tràng (xuất độ 6 lần đối với colon adenocarcinoma) hay u buồng trứng tiết nhày (mucin-secreting).
U nhày ruột thừa nên được xem là chẩn đoán phân biệt cho các khối vùng hố chậu P. Để có chẩn đoán chính xác trước mổ, bắt buộc phải làm CT. Tất cả nhằm giúp phẫu thuật viên cẩn thận hơn để tránh làm vỡ u nhày ruột thừa làm rò chất nhày vào ổ bụng gây giả u nhày phúc mạc.
Xem ca 181 Vietnamese Medic Ultrasound .
Tài liệu tham khảo chính:
Aghahowa EJ, Bharati C, Al-Adwani M: Appendicular Mucocele, A Case Report, Kuwait Medical Journal, March, 2008, pp78-8
Francica G, Lapiccirella G, Giardiello C, Scarano F, Angelone C, De Marino F, Molese V: Giant Mucocele of the Appendix, J Ultrasound Med, 2006, 25:643-648.0.
Đăng ký:
Bài đăng
(
Atom
)