Radiomics là một chuyên ngành khá mới liên quan đến việc trích xuất thông lượng cao các đặc điểm hình ảnh từ các hình ảnh y khoa [1-3]. Chúng được kết hợp với dữ liệu di truyền và lâm sàng, qua sử dụng các phương pháp trí tuệ nhân tạo để trích xuất các đặc điểm của khối u dựa trên sinh lý bệnh, sinh học phân tử và các thông tin liên quan khác, cung cấp các thực hành lâm sàng để hỗ trợ việc ra quyết định điều trị [4,5]. Hiện nay, radiomics có vai trò cần thiết trong chẩn đoán phụ trợ bệnh lý, dự đoán hành vi sinh học của khối u và đánh giá đáp ứng điều trị. Đã có một số nghiên cứu radiomics về chụp cắt lớp vi tính (CT), chụp cộng hưởng từ (MRI) và bệnh học [6-9]. Là một nhánh quan trọng của hình ảnh y khoa, siêu âm là một phương pháp tạo hình thời gian thực, năng động và thuận tiện, không gây tổn thương bức xạ và phạm vi bao phủ rộng và nhiều chế độ hình ảnh [10]. Radiomics ultrasound là một công nghệ phát triển nhanh chóng với những thách thức và cơ hội đáng kể. Cho đến nay, đã có những nghiên cứu trong nhiều lĩnh vực khác nhau như tuyến giáp [11], vú [12], gan [13], sản khoa [14], tuyến tiền liệt [15] và trực tràng [8]. Với những cập nhật liên tục trong công nghệ xử lý hình ảnh và ứng dụng các thuật toán máy học (ML), radiomics ultrasound có triển vọng ứng dụng rộng rãi. Các đặc điểm radiomics không chỉ tương quan với dữ liệu bộ gen mà còn cung cấp thông tin bổ sung liên quan đến tính không đồng nhất của u trên toàn khối u để tiên lượng sống còn và phân tầng nguy cơ. Trong thời đại y học được cá nhân hóa, ultrasound-based radiomics có tiềm năng cải thiện khả năng chẩn đoán, tiên lượng và đánh giá đáp ứng điều trị.
Ứng dụng lâm sàng của US-based radiomics
Trong thực hành lâm sàng, US được sử dụng rộng rãi để phát hiện các bất thường về hình thái các cơ quan (Bảng I). Với sự phát triển của US-based radiomics, nhiều dấu ấn sinh học hình ảnh sẽ xuất hiện thông qua việc trích xuất sâu hơn hình ảnh không thể nhìn thấy bằng mắt thường, cho phép chẩn đoán bệnh không xâm lấn sớm hơn và chính xác hơn.
Phân biệt lành tính và ác tính
Việc sử dụng phổ biến nhất của US-based radiomics là phân biệt giữa khối u lành tính và ác tính.
Do vị trí nông của tuyến giáp và chất lượng hình ảnh US cao US based radiomics được áp dụng trước tiên để phân biệt giữa nhân giáp lành tính và ác tính [38-41]. Zhang và cộng sự [11] đã trích xuất các đặc điểm radiomics từ 2064 hình ảnh US đàn hồi và B mode được xác nhận về mặt bệnh lý của các nhân tuyến giáp và thiết lập mô hình chẩn đoán bằng cách sử dụng thuật toán random forest algorithm /rừng ngẫu nhiên/. Khả năng phân biệt nhân giáp lành tính và ác tính của mô hình này tốt hơn so với các bác sĩ hình ảnh có kinh nghiệm. Tương tự, có một số nghiên cứu về US based radiomics để chẩn đoán các khối u lành tính và ác tính ở vú, một số nghiên cứu chỉ trích xuất các đặc điểm US từ hình ảnh B-mode , trong khi những nghiên cứu khác kết hợp giữa hình ảnh B-mode và elastography [42,43]. Các đặc điểm của bệnh ung thư vú triple negative ở US không điển hình. Lee và cộng sự [44] đã phân biệt thành công ung thư vú triple negative với fibroadenoma vú bằng cách sử dụng phân tích cấu trúc. Hệ thống Dữ liệu và Báo cáo Hình ảnh Vú (BI-RADS) là một phương pháp tiêu chuẩn để đánh giá các nốt ở vú. Tuy nhiên, sự khác biệt đáng kể giữa intra-observer và inter-observer dựa trên BI-RADS đã được báo cáo [45]. Luo và cộng sự [46] đã nghiên cứu 315 trường hợp tổn thương vú nguy cơ cao với BI-RADS 4 hoặc 5 và thiết lập mô hình dự đoán dựa trên radiomics kết hợp với phân loại BI-RADS. Mô hình cho thấy mức độ phân biệt cao giữa lành tính và ác tính (AUC 0,928; CI 95% [0.876, 0.908]).
Tổn thương gan lan toả
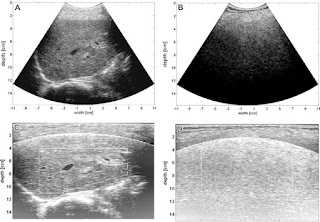
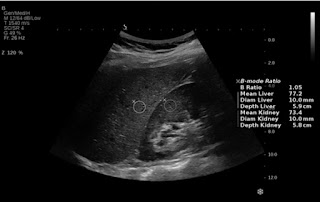
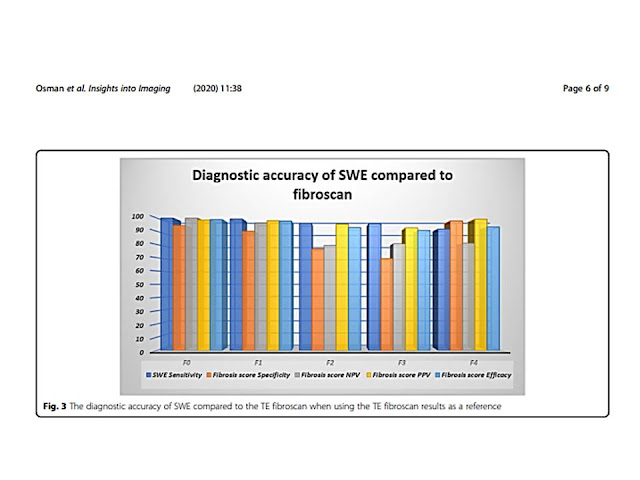
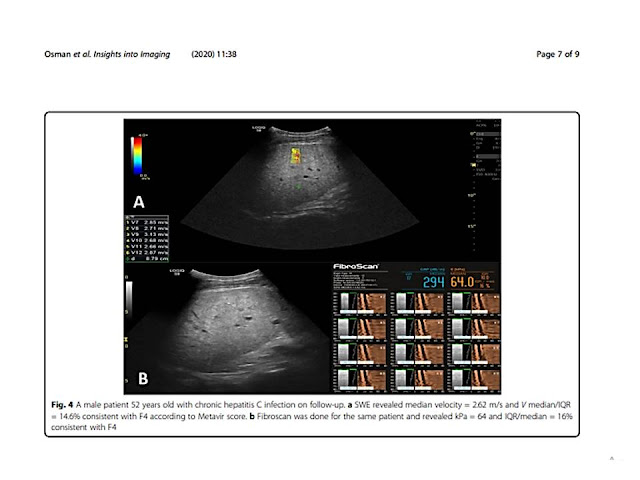
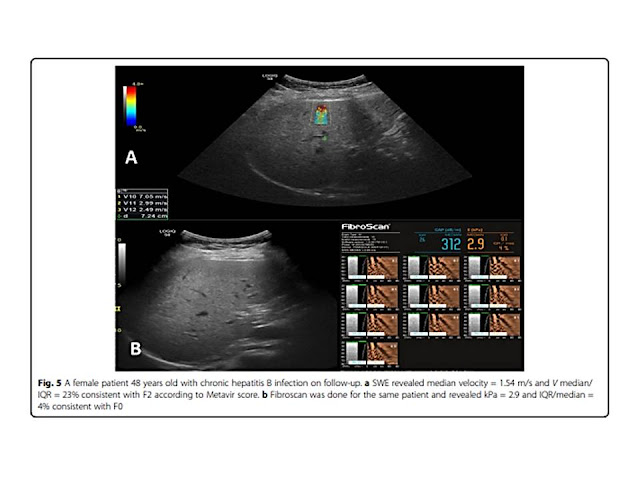
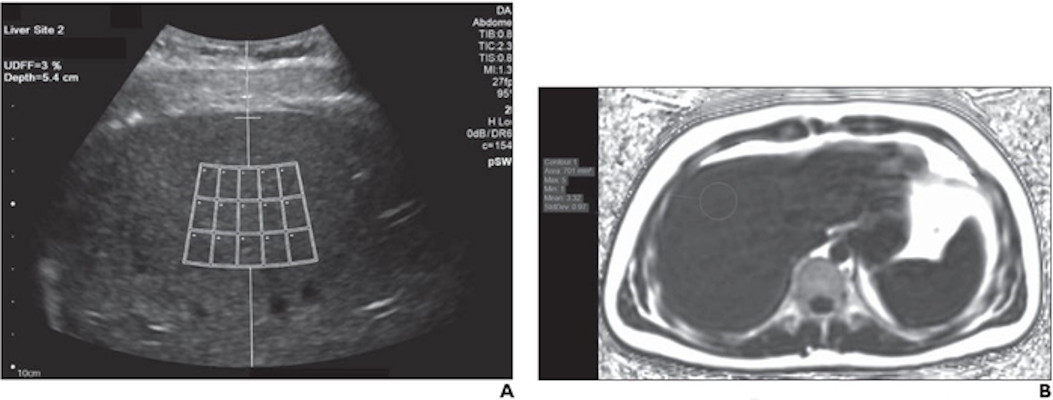
Cho đến nay, sinh thiết gan vẫn là tiêu chuẩn vàng để phân loại xơ hóa gan. Tuy nhiên, sinh thiết là thủ thuật xâm lấn và sai số lấy mẫu có ảnh hưởng đến kết quả. Ngoài ra, sinh thiết gan gây chảy máu, nhiễm trùng và các biến chứng nghiêm trọng khác. Do đó, một số nghiên cứu đã sử dụng US based radiomics để phân loại xơ hóa gan. Các phương thức và thuật toán ML khác nhau của US đã được sử dụng để dự đoán phân loại xơ hóa gan, và tất cả đều có độ chính xác chẩn đoán tốt [37,54-56]. Một nghiên cứu tiền cứu đa trung tâm [57] sử dụng DL trên US đàn hồi sóng biến dạng (SWE) của gan đã báo cáo hiệu quả chẩn đoán cải thiện đáng kể để đánh giá xơ hóa gan trong viêm gan B mạn tính, với khả năng chẩn đoán xơ hóa gan F4 và ≥F3 tiến gần đến mức giải phẫu bệnh lý.
Liu và cộng sự [58] đã sử dụng mạng thần kinh phức hợp để phân tích các đặc điểm hình ảnh radiomics của bao gan và sau đó sử dụng SMV để phân biệt bệnh nhân xơ hóa gan; AUC đạt 0,92.
Tang và cộng sự [59] đã phát triển một mô hình ML dựa trên các thông số định lượng của US bằng cách sử dụng SWE ở chuột và độ chính xác phân loại của bệnh viêm gan nhiễm mỡ được cải thiện đáng kể.
Đánh giá các hành vi sinh học của khối u và cấu hình phân tử
Tiến triển của ung thư đi kèm với những thay đổi sinh lý và sinh hóa phức tạp trong khối u và mô xung quanh. Các đặc điểm hình thái của tổn thương nguyên phát có mối quan hệ nhất định với hành vi sinh học của khối u, chẳng hạn như di căn hạch, độ xâm lấn, mức độ bệnh lý và sự biệt hóa [60]. Tuy nhiên, một số đặc điểm hình thái vi mô này không thể nhìn thấy bằng mắt thường. Các dấu ấn sinh học hình ảnh dự kiến sẽ được trích xuất thông qua phân tích radiomics và hành vi sinh học của những tổn thương này có thể được đánh giá không xâm lấn trước phẫu thuật. Di căn hạch là cơ sở cần thiết cho việc phân giai đoạn di căn hạch (TNM). Xác định di căn hạch trước phẫu thuật có tầm quan trọng lớn trong việc lựa chọn phương pháp điều trị và tiên lượng bệnh nhân [61].
Một số nghiên cứu đã chứng minh mối quan hệ chặt chẽ giữa các đặc điểm hình ảnh khối u và di truyền học, có thể cung cấp cơ sở sinh học cho ứng dụng lâm sàng của xạ hình [3]. Gần đây, Kwon et al [70] đã thực hiện một phân tích siêu âm radiomics từ 96 trường hợp PTC được xác nhận bởi bệnh lý; 86 tính năng radiomics đã thu được và một mô hình dự đoán được thành lập, cho thấy hiệu suất vừa phải và dự đoán đột biến BRAF trong PTC. Tuy nhiên, trong một nghiên cứu [71], các đặc điểm radiomics được trích xuất từ 527 hình ảnh của US cho thấy giá trị hạn chế như một dấu ấn sinh học không xâm lấn để dự đoán sự hiện diện của đột biến BRAF V600E của PTC không tinh kích thước.
Các đặc điểm radiomics cung cấp các dấu ấn sinh học có giá trị. Có một số phân tích định lượng về hình ảnh của US phản ánh sinh học khối u ở tế bào và mức độ phân tử. Guo và cộng sự [72] đã chứng minh rằng các đặc điểm US radiomics được trích xuất từ hình ảnh ung thư vú có thể phân biệt các khối u có biểu hiện thụ thể estrogen và progesterone khác nhau (AUC = 87,7%). Vi mạch xâm lấn (MVI) [73], được định nghĩa là sự xâm lấn của các tế bào u trong một không gian mạch máu được lót bởi nội mô, đã được chứng minh rộng rãi như một yếu tố dự báo tái phát sớm của ung thư biểu mô tế bào gan (HCC). Hu et al [74] đã trích xuất các đặc trưng của radiomics US của 482 bệnh nhân mắc ung thư biểu mô tế bào gan trên US và thành lập mô hình dự đoán lâm sàng-X quang kết hợp AFP và kích thước khối u, cho thấy một giá trị dự đoán tuyệt vời cho MVI positivity.
Tương tự, Yao và cộng sự [75] đã thực hiện một phân tích radiomics hình ảnh đa phương thức của US của 177 bệnh nhân tổn thương gan, trích xuất các đặc điểm radiomics và thiết lập năm mô hình ML, cho thấy hiệu suất chẩn đoán và dự đoán tốt để phân biệt lành tính và ác tính và mức độ của các dấu ấn sinh học như như PD-1, Ki-67 và MVI. Ung thư đường mật (ICC) là một bệnh ung thư nguyên phát tích cực có nguồn gốc trong biểu mô ống mật chủ [76]. Không giống như HCC, phẫu thuật cắt bỏ hiện là phương pháp điều trị duy nhất cho bệnh nhân ICC [77]. Một nghiên cứu [78] đã trích xuất các đặc điểm radiomics tiên đoán nhất để đánh giá MVI, xâm nhập perineural, biệt hóa, Ki-67, VEGFR và CK7 trong ICC và báo cáo rằng các tính năng này có hiệu quả vừa phải trong việc dự đoán không xâm lấn hành vi sinh học của ICC.
Tumor deposits/Khối u lắng đọng (TDs) trong ung thư trực tràng được định nghĩa là các focal clusters/cụm tiêu điểm/ của ung thư biểu mô tuyến nằm ở quanh trực tràng hoặc mỡ quanh trực tràng gần khối u nguyên phát và không kết hợp với khối u nguyên phát hoặc các hạch bạch huyết [79]. TDs có liên quan đến giai đoạn TNM. TD positive có nghĩa là khối u hung hãn hơn và tiên lượng xấu hơn. Rất khó để chẩn đoán xác định TD positive bằng hình ảnh thông thường và chỉ có thể xác định được bệnh lý hậu phẫu. Chen và cộng sự [80] đã phân tích US và độ đàn hồi các đặc điểm hình ảnh của US của 127 bệnh nhân ung thư trực tràng và tiên lượng tiền phẫu của TD-positive.
Ra quyết định điều trị và đánh giá tiên lượng
Cắt bỏ phẫu thuật (SR) và cắt bỏ bằng tần số vô tuyến (RFA) là hai chiến lược điều trị chính để chẩn đoán ung thư biểu mô tế bào gan sớm [81]. Tuy nhiên, sự lựa chọn điều trị cho cá nhân vẫn còn tranh cãi. Liu et al [82] tối ưu hóa việc điều trị HCC sớm dựa trên DL của radiomics trong CEUS, không chỉ dự đoán tỷ lệ sống không tiến triển (progression-free survival, PFS) của bệnh nhân RFA và SR nhưng cũng xác định rằng 17,3% bệnh nhân RFA và 27,3% bệnh nhân SR cần được trao đổi các lựa chọn, có thể làm tăng PFS 2 năm lần lượt là 12% và 15%. Liu và cộng sự [83] đã phát triển và xác thực mô hình radiomics DL dựa trên CEUS (R-DLCEUS), một mô hình ML dựa trên radiomics của đường cong cường độ thời gian CEUS (R-TIC) và ML dựa trên radiomics của hình ảnh thang xám (chế độ R-B) để dự đoán đáp ứng điều trị của bệnh nhân ung thư biểu mô tế bào gan sau khi cá nhân hóa hóa trị liệu động mạch qua gan. Các R-DLCEUS đã báo cáo hiệu quả chẩn đoán cao nhất của 0,93 (KTC 95%, 0,80-0,98) và có thể đạt được hiệu quả dự đoán chính xác và được cá nhân hóa. Tương tự, Ma et al [84] đã phát triển một mô hình kết hợp dựa trên tiền phẫu thuật hình ảnh CEUS động, US thường quy và các yếu tố lâm sàng của tổn thương HCC để dự đoán tái phát sớm và muộn ở bệnh nhân có một tổn thương HCC đơn lẻ có đường kính ≤5 cm sau khi cắt đốt bằng nhiệt, cho thấy hiệu quả tốt (nhóm huấn luyện: AUC 0,89, nhóm thử nghiệm: AUC 0,84). Park và cộng sự [85] đã đánh giá và dự đoán khả năng sống không bệnh của PTC dựa trên các đặc điểm radiomics B-mode US, dự kiến sẽ cung cấp được chẩn đoán và điều trị cá nhân hóa, và giảm đi việc điều trị quá mức ung thư tuyến giáp. Các nghiên cứu về US radiomics hiện tại chủ yếu dựa trên hình ảnh từ một thời điểm duy nhất, trong khi hiệu quả điều trị được dự đoán thông qua phân tích so sánh hình ảnh từ nhiều mốc thời gian trong quá trình điều trị. Một nghiên cứu đa trung tâm cho thấy rằng US radiomics có thể theo dõi đáp ứng điều trị với neoadjuvant chemotherapy/ hóa trị bổ trợ tân sinh/ ở ung thư vú tiến triển tại chỗ.
Tồn tại và cơ hội trong tương lai
Dựa theo điểm đánh giá chất lượng radiomics [87], hình ảnh chất lượng cao, thu thập dữ liệu được chuẩn hóa và xử lý, thêm thông tin từ hình ảnh mới của nhiều thời điểm hơn, nghiên cứu dựa trên cơ sở sinh học phân tử và bệnh học có thể cải thiện chất lượng của các nghiên cứu về radiomics[19].
Các phần tương đối không cố định của US, sự phụ thuộc vào người khám và sự không nhất quán của cài đặt thiết bị và thông số là những lý do chính tại sao sự phát triển của radiomics không theo kịp sự phát triển của các phương pháp chẩn đoán hình ảnh y khoa khác. Ngoài ra, các tính năng của US chỉ có thể được trích xuất từ một phần của tổn thương, vì vậy nó không thể phản ánh toàn bộ khối u, cũng là một hạn chế của việc áp dụng phương pháp US radiomics. Hiện tại, số lượng hình ảnh trong hầu hết các nghiên cứu US radiomics là hàng trăm, vẫn chỉ là số nhỏ khi thực tế là hàng nghìn trường hợp. Hơn nữa, hầu hết là nghiên cứu đơn độc, điều này làm hạn chế tính tổng quát của các mô hình ML. Phần lớn các nghiên cứu dựa trên US radiomics là hồi cứu.
Thiết kế tương lai có thể cải thiện chất lượng của nghiên cứu nhưng cần khối lượng công việc và thời gian nhiều hơn. Một thách thức khác là khả năng giải thích giữa các đặc điểm hình ảnh radiomics được trích xuất hiện tại và các đặc điểm lâm sàng.
Với sự cải tiến của công nghệ xử lý hình ảnh, phát triển các phương pháp trí tuệ nhân tạo phù hợp với máy US và liên tục cải tiến độ phân giải của thiết bị, US radiomics đã gia tăng triển vọng. DL đã được chứng minh là cải thiện hiệu suất đáng kể so với các phương pháp ML truyền thống [88]. TL cũng là một phương pháp hiệu quả để phân loại các cơ sở dữ liệu tương đối nhỏ hiện có. TL đã được đề xuất để có thể áp dụng nhiều hơn trong phân tích hình ảnh US radiomics.